鐵基鋰離子電池材料研究進展
胡友作譚銘劉珊珊舒小會張美玲劉興泉
電子科技大學(xué)微電子與固體電子學(xué)院,成都610054
摘要:Fe是地球上儲存含量最多的金屬,相較于已商業(yè)化的鋰離子電池正負極材料,Fe基電池材料來源豐富、成本較低、無毒無污染、對環(huán)境友好、安全性能好,并且既可以用作正極材料也可用作負極材料。因此,很多鐵基化合物被當(dāng)做鋰離子電池材料研究過,本文選擇了LiFeO2,LiFePO4,Fe3O4和Fe2O3等幾種較熱門的鐵基正負極材料進行性能和制備方法的綜述。
關(guān)鍵詞鐵基電極材料;LiFeO2;LiFePO4;Fe3O4;Fe2O3
Research Advances on Fe-based Cathode Materials for Lithium-ion Batteries
HU You-zuo, TAN Ming, LIU Shan-shan, SHU Xiao-hui, ZHANG Mei-ling,
LIU Xing-quan*
School of Microelectronics and Solid State Electronics, University of Electronic Science and Technology of China, Chengdu 610054, Sichuan China.
Abstract:Iron(Fe)is the most abundant metal in the world,Comparing with those commercial lithium ion battery electrode materials, iron-based materials are low cost, nontoxic, environmental friendliness and good safety which can be used as alternatives of cathode material or anode material.Therefore,lots of iron-based materials have been researched as electrode material of high power lithium ion batteries.In this work ,we report the performance and synthesis route of LiFeO2,LiFePO4,Fe3O4 and Fe2O3,which popularly be researched as cathode and anode material of lithium ion batteries.
Keywords:iron-based materials;LiFeO2;LiFePO4;Fe3O4;Fe2O3
引言
隨著社會的不斷發(fā)展,傳統(tǒng)能源不僅給環(huán)境帶來污染,而且資源日趨枯竭,因此人們對新能源的渴求不斷加強。鋰離子電池作為純動力汽車和混合動力汽車以及便攜式移動電子產(chǎn)品的主要供能系統(tǒng),其應(yīng)用不斷多元化,為了滿足新的應(yīng)用需求,電池的容量,能量密度和循環(huán)壽命等都需要進一步提升。目前,商業(yè)化的鋰離子電池正極材料主要有LiCoO2、LiNiO2和LiMnO2。其中LiCoO2是應(yīng)用最廣泛的正極材料,但鈷資源稀缺、價格昂貴,其毒性大對環(huán)境有害。雖然LiCoO2的理論容量高達274mAh×g-1,但在實際應(yīng)用中容量只能達到140mAh×g-1。LiNiO2具有與LiCoO2相似的層狀結(jié)構(gòu),實際容量可達190-210mAh×g-1,循環(huán)性能良好,但合成困難,產(chǎn)品質(zhì)量不高,且在循環(huán)充放電時結(jié)構(gòu)容易坍塌,熱穩(wěn)定性和安全性差。尖晶石結(jié)構(gòu)的LiMn2O4原材料豐富,價格低廉,對環(huán)境友好,但理論容量只有148mAh×g-1,可逆容量在120mAh×g-1左右。且容易發(fā)生Jahn-Teller效應(yīng)致使容量快速衰減[1]。負極方面,鋰離子電池作為新型的高能電池性能上的提高仍有很大空間,而負極材料性能的提高是其中的關(guān)鍵,目前主要的負極材料有碳,鋰過渡金屬氮化物,過渡金屬氧化物等。層狀結(jié)構(gòu)碳負極對電解液高度敏感,與溶劑相容性差,鋰過渡金屬氮化物充放電曲線不太穩(wěn)定,過渡金屬氧化物容量衰減較快,放電曲線不穩(wěn)定[2]。為了改善已有正負極材料的缺點,推動鋰離子電極材料朝高能量密度、低成本、高安全性、高質(zhì)量和良好的循環(huán)性能等方向發(fā)展,國內(nèi)外相關(guān)機構(gòu)都投入了大量人力物力研究新型鋰離子電池的電極材料。鐵作為地球上儲存含量最豐富的元素,其價格低廉,無毒性對環(huán)境友好,因此,鐵基電極材料正在受到越來越多的關(guān)注,本文針對LiFeO2,LiFePO4兩種較重要的正極材料和常被用作負極的Fe3O4和Fe2O3的制備方法和結(jié)構(gòu)性能進行綜述。
1 LiFeO2的性能特點和制備方法
LiFeO2具有多種不同的晶型,如圖1所示。主要有α-LiFeO2、β- LiFeO2、γ-LiFeO2、波紋狀LiFeO2、四面體型t-LiFeO2、錳鋇礦型LiFeO2、針鐵礦LiFeO2。α-LiFeO2是陽離子無序的立方巖鹽結(jié)構(gòu),屬于Fm3m空間群。β-LiFeO2屬C2/c空間群。γ-LiFeO2屬于I41/amd空間群,為四方結(jié)構(gòu)。波紋狀LiFeO2屬Pmnm空間群,是正交晶體結(jié)構(gòu)。四面體型t-LiFeO2屬于Pna21空間群。錳鋇礦型LiFeO2屬于I4/m空間群,為四方晶體結(jié)構(gòu)。針鐵礦LiFeO2屬于Pbnm空間群,是正交晶體結(jié)構(gòu)。在實驗中可以通過不同的制備方法得到不同結(jié)構(gòu)的LiFeO2,目前主要的制備方法包括高溫固相法、低溫熔鹽法、水熱合成法、溶劑熱合成、離子交換法和低溫固相法等。一般超過600℃合成的LiFeO2電化學(xué)活性較低,具有良好電化學(xué)活性的LiFeO2都是通過低溫合成方法制得,具有電化學(xué)活性的LiFeO2首輪充放電曲線和后續(xù)充放電曲線不一致,對此的解釋主要集中在LiFeO2首輪充電時發(fā)生了結(jié)構(gòu)的轉(zhuǎn)變[3-4]。
Kanno等[4]在研究波紋層狀LiFeO2的性能時,發(fā)現(xiàn)初期容量衰減較快,由此推測結(jié)構(gòu)由波紋層狀向非結(jié)晶相轉(zhuǎn)變,隨后的充放電是在非結(jié)晶相LiFeO2中進行的。Lee等[5]人在150℃下,以LiOH×H2O和通過傳統(tǒng)固相法合成了LiFeO2,在電流密度為0.1mA/cm2,電壓平臺為4.5~1.5之間時對電池進行測試,如圖2(a)所示,發(fā)現(xiàn)第一次充放電曲線和后續(xù)充放電曲線有較大不同,通過原位XRD的進一步表征后發(fā)現(xiàn)初次充電的原位XRD圖譜如圖2(b)所示,其中有些峰會分裂為兩部分,有些峰有輕微的加強,初次放電的圖譜如圖2(c)所示,有較多的峰已經(jīng)轉(zhuǎn)變,2°的正交晶峰在2.3V時有所減少,隨后就不再出現(xiàn),除此之外一些主峰也在2.3V區(qū)域發(fā)生了改變,通過TEM的進一步表征發(fā)現(xiàn)初次循環(huán)時正交晶結(jié)構(gòu)的LiFeO2向尖晶石相的LiFe5O8轉(zhuǎn)變。Catti等[6]人對初次充放電和后續(xù)充放電的電化學(xué)反應(yīng)進行了假設(shè),初次充電反應(yīng)、初次放電反應(yīng)、后續(xù)充放電反應(yīng),通過第一性原理計算法證實發(fā)現(xiàn)在首次充電時Li從LiFeO2中脫出,使Fe部分氧化,導(dǎo)致LiFeO2結(jié)構(gòu)中有部分空位。在首次放電時,缺Li的鐵氧化物與Li反應(yīng)分解為尖晶石相的LiFe5O8,可見Li未在充電過程中回嵌入正極材料中。在后續(xù)充放電反應(yīng)中Li就在LiFe5O8中不斷嵌入和脫出,伴隨著Fe價態(tài)從3+到2.6+不斷變化。這也很好的解釋了LiFeO2首輪充放電曲線與后續(xù)的差異原因,也證實了后續(xù)的充放電反應(yīng)都在尖晶石相的LiFe5O8中進行。
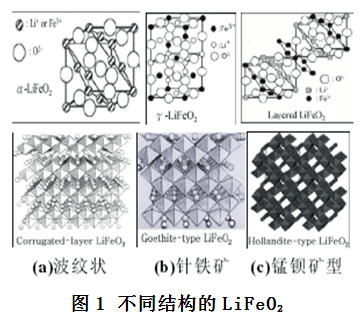
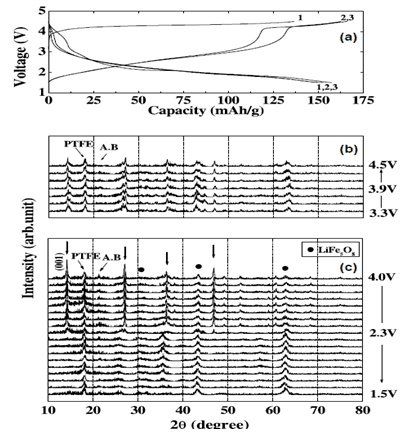
圖2 (a)LiFeO2充放電曲線(b)初次充電的原位XRD圖譜(c)初次放電的原位XRD圖譜
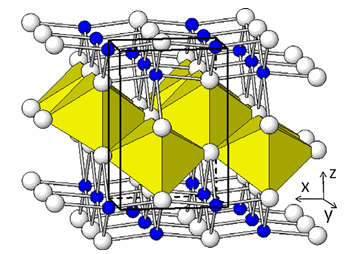
圖3 波紋層狀LiFeO2晶體結(jié)構(gòu),深藍色和白色分別為Li原子和O原子
Amstrong等人[7]通過離子交換法制備出四面體型t-LiFeO2,其容量可達120mAh×g-1,但是在循環(huán)過程中會由四面體型轉(zhuǎn)變成尖晶石相LiFe5O8,且伴隨著O的缺失,因為在脫嵌過程中Li+被H+置換導(dǎo)致H2O的生成,t-LiFeO2也在此過程中轉(zhuǎn)變尖晶石相LiFe5O8,反應(yīng)過程如下:
LiFeO2+xH+=Li(1-x)HxFeO2+xLi+
LiFeO2的另一個明顯特征就是通過減小粒徑、增大比表面積可以提高其電化學(xué)活性,Li等人通過低溫溶劑熱法制備出平均粒徑為80~100nm的α-LiFeO2,其電化學(xué)活性得到明顯提升。Wang等[8]以LiNO3和LiHO×H2O為原料,通過低溫熔鹽法制備出了納米棒狀LiFeO2,其電化學(xué)性能也得到明顯提升,作者認為這歸因于較小的粒徑促進了鋰的嵌入和脫出反應(yīng)。Wu等[9]用作為前驅(qū)物,通過離子交換法制備出了LiFeO2納米顆粒,在1.5~4.5V循環(huán)時,其可逆容量達到65~80mAh×g-1。Morales等[10]人通過固相球磨法制備了粒徑大于50nm的球狀LiFeO2納米顆粒,這些顆粒以束狀形式相互團聚,這樣成串的結(jié)構(gòu)為鋰離子提供了暢通的擴散通道,在1.5~4.5V循環(huán)時其容量達到150mAh×g-1。Hirayama等[11]先用水熱法合成納米級的NaFeO2顆粒,再用離子交換法合成平均粒徑為40nm的具有層狀巖鹽結(jié)構(gòu)的LiFeO2納米顆粒,其容量達到120mAhg-1。Liu等[12]人通過流變相法制備出高結(jié)晶度的α-LiFeO2,其平均粒徑分布在100~300nm之間,初始放電容量高達169mAhg-1,50次循環(huán)后容量保留率達96.8%。可見較小的顆粒尺寸可以促進鋰離子的擴散,改變其電化學(xué)性能。
為了改變LiFeO2在循環(huán)過程中結(jié)構(gòu)改變,低電壓下工作時電化學(xué)活性差,導(dǎo)致容量快速衰減,不可逆容量大等問題,人們通過包覆,制備固溶體和摻雜改性的方式改善其電化學(xué)性能。Zhang等[13]人通過固相反應(yīng)法制備出了聚吡咯包覆的α-LiFeO2,聚吡咯是比較常見的導(dǎo)電聚合物,可以儲存電荷,也可用作粘接劑,通過FESEM表征發(fā)現(xiàn)菜花狀的聚吡咯納米顆粒包覆在LiFeO2表面,減少了LiFeO2顆粒之間的表面接觸電阻,因此大大提高LiFeO2的電導(dǎo)性,LiFeO2在0.1C下的可逆容量和循環(huán)穩(wěn)定性得到提升,在100次循環(huán)后容量為104mAhg-1。Lee Y.S[14]等人以LiOH.H2O,為原料通過傳統(tǒng)固相反應(yīng)法,然后分別在150℃和350℃下燒結(jié)所得樣品,通過XRD表征發(fā)現(xiàn)150℃下燒結(jié)得來的樣品只是LiFeO2和錳氧化物的混合物,而在350℃下燒結(jié)得到的樣品為LiFeO2-LixMnO2固溶體。對Mn含量為10%,30%和50%的固溶體進行測試后發(fā)現(xiàn),隨著Mn含量的增加材料循環(huán)性能和容量都在改善,Mn含量為50%時,初始容量達到140mAhg-1,且在2.8V出現(xiàn)電壓平臺,這被認為是在低電壓下Mn發(fā)生了Mn4+/Mn3+的氧化還原反應(yīng),進一步鞏固了材料的結(jié)構(gòu),提高其循環(huán)性能。Matasuhara等[15]人以LiOH×H2O、Fe2O3和輝鉬礦為原料,通過固相反應(yīng)法得到前驅(qū)物,然后再研磨混合壓制成片狀,在1050℃空氣中加熱24小時,合成xLi4MoO5×(1-x)LiFeO2固溶體,x=0.5時得到單相Li1.42Mo0.29Fe0.29O2,初始容量可以達到350mAh×g-1。Suresh等[16]先以溶液氧化法制備出NaFeO2和NaFe0.9Co0.1O2前驅(qū)物,然后通過Na+/Li+離子交換法制得LiFeO2和LiFe0.9Co0.1O2,兩種材料初始容量都達到205mAh×g-1,但LiFeO2在循環(huán)5次后衰減到140mAh×g-1,而LiFe0.9Co0.1O2循環(huán)30次后容量還有190mAh×g-1,作者由此認為Co的存在起到了穩(wěn)定層狀結(jié)構(gòu)的作用,從而使其循環(huán)性能更好。
2 LiFePO4的性能特點和制備
LiFePO4理論容量為170mAh×g-1,價格低廉,環(huán)境友好,無毒性,是一種非常有應(yīng)用前景的正極材料,并得到了廣泛的關(guān)注,相對金屬鋰的電極電位為3.45V。具有有序的橄欖石型結(jié)構(gòu),如圖3所示,屬于正交晶系Pmnb群,每個晶胞中有四個LiFePO4單元,氧原子以近似六方密堆積,磷原子在氧四面體的4C位,鐵原子和鋰原子在氧八面體的4C和4a位,FeO6八面體在b-c平面通過共點連結(jié)起來。一個FeO6八面體和兩個LiO6八面體和一個PO4四面體共棱,Li+在4a位形成共棱的連續(xù)直線鏈并平行于C軸,這樣Li+具有二維可移動性,可以在充放電過程中自由脫出和嵌入。LiFePO4中O2-和P5+形成PO43-的聚合四面體穩(wěn)定了整個三圍結(jié)構(gòu),從而使其在高溫下更穩(wěn)定更安全。LiFePO4循環(huán)性能較好,充放電過程中晶體結(jié)構(gòu)穩(wěn)定,充放電曲線很長很平穩(wěn)[17-18]。
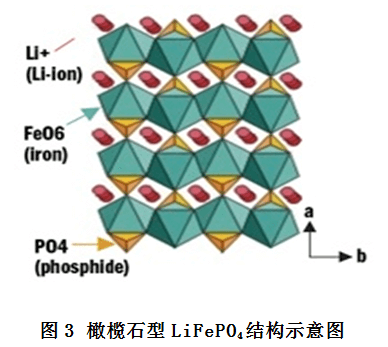
LiFePO4雖然具有良好的性能,但其固有電導(dǎo)率和鋰離子擴散系數(shù)均較低,合成方法的不同會極大影響LiFePO4的電化學(xué)性能,目前常見的合成方法有高溫固相法、溶膠-凝膠法、水熱合成法、共沉淀法等[18]。Takahashi等[19]人在675℃下通過固相合成制備出了粒徑相對較小,表面較粗糙的LiFePO4顆粒,相對更高溫度下得到的產(chǎn)物,其晶體結(jié)構(gòu)完好,電化學(xué)性能更良好。Bollju等[20]人通過水熱合成法,將鐵粉作為鐵源制備出了結(jié)構(gòu)完好的LiFePO4,在0.1C倍率下容量達165mAh×g-1。相較于用二價鐵鹽合成前驅(qū)體再進一步合成的LiFePO4,此種水熱合成法較經(jīng)濟實惠和對環(huán)境友好。Tian等[21]人通過共沉淀法制備了多孔LiFePO4,發(fā)現(xiàn)三維多孔結(jié)構(gòu)增加了材料的接觸表面積,減少了鋰離子的擴散距離,提高電荷遷移速率,在鋰離子循環(huán)脫嵌過程中保持了穩(wěn)固的結(jié)構(gòu),有利于鋰離子的脫嵌,其容量達到167mAh×g-1,經(jīng)過300次循環(huán)后容量保留率為99.3%。Gao等[22]人用單模式微波水熱合成法制得循環(huán)穩(wěn)定性較好的橄欖石型的六邊LiFePO4納米片,制備過程中微波輻射可以有效減少合成溫度和時間。
在使用過程中LiFePO4主要的問題是電導(dǎo)率低,因此通過合成工藝提高其電導(dǎo)率,改善材料性能非常關(guān)鍵。目前主要用的方法是通過表面改性提高LiFePO4的電導(dǎo)性,包括碳包覆,添加金屬粉體誘導(dǎo)成核,包覆具有導(dǎo)電性的金屬化合物[18]。Tu等[23]人通過冷凍干燥法制備出了與摻雜氮的碳納米管互相融合,且均勻分散的三圍多孔LiFePO4,通過表征發(fā)現(xiàn)氮摻雜的碳納米管均勻分布在LiFePO4的孔隙中,構(gòu)成了完善的三圍導(dǎo)電網(wǎng)絡(luò)結(jié)構(gòu),大大提高了LiFePO4循環(huán)穩(wěn)定性和電導(dǎo)率,其庫倫效率達到97.75%。Prosini等[24]人在制備LiFePO4時加入了高比表面的炭黑,加入的碳粉均勻的分散在LiFePO4顆粒之間有助于細化LiFePO4顆粒,增加其電導(dǎo)率和循環(huán)性能。在80℃,C/10下的放電倍率為170mAh×g-1,室溫下進行230次循環(huán)后容量為95mAh×g-1。Milev等人[25]通過水熱法添加維生素C和檸檬酸制備出了片狀LiFePO4/C納米復(fù)合物,維生素C和檸檬酸在高溫煅燒時可以充當(dāng)還原劑阻止鐵氧化物的生成。此外,剩余的碳還能阻止晶粒的過渡生長,控制產(chǎn)物的形貌,并且提高了材料的導(dǎo)電率,使其容量達到164.3mAh×g-1。Zhao等[26]人通過固相反應(yīng)法對LiFePO4進行硅摻雜和碳包覆,硅元素取代了部分LiFePO4晶格中的P元素,可以提高LiFePO4的電導(dǎo)率,同時碳包覆可以減少LiFePO4與電解液之間的表面熱阻,在5C倍率下的放電容量為119mAh×g-1,10C倍率下的容量為94mAh×g-1。除了碳包覆可以提高材料的導(dǎo)電性能,通過包覆金屬粉體,包括Cu、Ag、Au等也會提高材料的導(dǎo)電性能而不降低粉體材料的振實密度和結(jié)構(gòu)。Goktepe等[27]人用銀和碳對LiFePO4進行雙重包覆,表征發(fā)現(xiàn)銀和碳并未改變LiFePO4的結(jié)構(gòu),包覆顆粒均勻分散在LiFePO4顆粒表面,兩種包覆材料的協(xié)同效應(yīng)使得鋰離子的擴散率和LiFePO4的電導(dǎo)率得到提高,同時又減小了材料的顆粒尺寸。Johnson等[28]人選擇鈮進行摻雜,用水熱合成法制備了LiFePO4納米顆粒。SEM面掃描結(jié)果顯示鈮在LiFePO4顆粒表面均勻分散,LiFePO4的電化學(xué)性能隨著鈮的增加而不斷改善,鈮添加量達到1%時,在10C倍率下放電容量達到110mAh×g-1。Saroha等[29]人通過溶膠凝膠法和固相球磨法制備出了氧化鋅摻雜的LiFePO4,所得樣品都屬于Pnma空間群的正交晶相,在氧化鋅的摻雜量達到2.5%和5%時LiFePO4仍然能夠保持結(jié)構(gòu)不變,靜電力顯微鏡顯示氧化鋅摻雜的LiFePO4電子電導(dǎo)率和鋰離子擴散速度更快,放電容量和循環(huán)性能也較好,0.1C倍率下放電容量為164mAh×g-1,在50次循環(huán)后容量保持率為95%,可見金屬氧化物摻雜也會提高LiFePO4的性能
3 其他鐵基正極材料的性能和制備條件
LiFeO2和LiFePO4是目前被研究最多的鐵基電極材料,并且基本都用作正極材料。除了以上兩種正極材料外,Fe3O4、Fe2O3也是目前被研究較多的電極材料,Fe3O4具有反尖晶石結(jié)構(gòu),其中的Fe既有正三價也有正二價,氧離子采取立方緊密堆積方式排列,鐵離子則占據(jù)四面體或八面體間隙位置,其理論容量為928mAh×g-1,主要制備方法包括低溫液相法、溶劑熱法、水熱法等,由于Fe3O4既有正三價也有正二價,所以在合成過程中得引入還原劑。Fe3O4具有較高的理論比容量,但為了進一步增加其電導(dǎo)性和循環(huán)性能通常對其進行碳包覆改性[2]。
Muraliganth等[30]人用微波水熱合成法制備了碳包覆單晶Fe3O4納米線和純單晶Fe3O4納米線,發(fā)現(xiàn)純Fe3O4初始容量為1240mAh×g-1,在循環(huán)中不斷衰減,經(jīng)過50次循環(huán)后容量保留率為50%,而碳包覆的Fe3O4初始容量為830mAh×g-1,經(jīng)過50次循環(huán)后容量保持100%,沒有絲毫損失,循環(huán)性能的提高主要是因為碳層在納米線里形成緩沖層,阻止了相鄰納米線的接觸,因此減少了納米線在循環(huán)過程中的衰減。Zhou等[31]人通過水熱法制備了石墨烯包覆的Fe3O4,石墨烯為均勻分散的Fe3O4顆粒提供了較大的接觸面積,促進了電子傳輸速率,提高其循環(huán)性能,在100次循環(huán)后容量為700mAh×g-1。
Fe2O3具有剛玉結(jié)構(gòu),陽離子采取六方緊密堆積方式排列,鐵離子占據(jù)三分之二的八面體間隙位置,其理論容量為1005mAh×g-1,制備方法主要包括液相法、熱氧化及熱分解法、電化學(xué)方法等。Fe2O3被用作負極材料時體積會隨著鋰離子的脫嵌而出現(xiàn)大幅度的膨脹收縮,這會導(dǎo)致容量衰減過快和循環(huán)穩(wěn)定性差[2]。Li等[32]人通過水熱合成法制備了多孔中空的納米Fe2O3,中空的納米材料一方面可以擴大電解液和電極材料之間的接觸面積,以縮短鋰離子的擴散通道,另一方面材料中的空隙位可以協(xié)調(diào)鋰離子脫嵌過程中材料體積的改變和結(jié)構(gòu)應(yīng)力,在50次循環(huán)后其容量為870mAh×g-1。Yang等[33]人通過一步機械球磨法制備Li2CO3包覆的具有分層結(jié)構(gòu)的納米晶Fe2O3,1~3nm厚的Li2CO3薄膜均勻包覆在Fe2O3表面,表現(xiàn)出了良好的循環(huán)穩(wěn)定性,其初始容量為985mAh×g-1,400次循環(huán)后容量為975mAh×g-1。
4 結(jié)語
鐵基鋰離子電池材料不僅材料來源豐富,且無毒對環(huán)境友好,不僅可以用作正極材料也可用作負極材料,其理論容量和已商業(yè)化的電極材料較接近,是目前被研究較多的電極材料。本文選擇LiFeO2和LiFePO4兩種熱門鐵基正極材料和多被用作負極材料的Fe3O4和Fe2O3進行綜述,LiFeO2具有多種晶型,可以通過不同的制備方法得到不同結(jié)構(gòu)材料,在用作正極材料時理論容量較高,但存在循環(huán)過程中結(jié)構(gòu)轉(zhuǎn)變,目前人們多采用減小粒徑,包覆或摻雜等方式進行改性,并得到較好效果。LiFePO4不僅容量較高,且循環(huán)性能良好,早已被商業(yè)化,目前對其性能的改進主要集中在電導(dǎo)率低的問題上。Fe3O4和Fe2O3一般用作鋰離子電池負極材料,與已經(jīng)商業(yè)化的負極材料相比兩者都具有較高的容量和結(jié)構(gòu)穩(wěn)定性,目前研究者通過多種改性方式進一步提高Fe3O4和Fe2O3的電導(dǎo)性和循環(huán)穩(wěn)定性。綜上所述,鐵基材料具備的獨特優(yōu)勢,很好的迎合了目前人們對鋰離子電池高密度高能量,對環(huán)境友好等性能的要求和渴望,將會進一步被研究并成為新一代鋰離子電池電極材料。
參考文獻
[1]M. Stanley Whittingham.Lithium Batteries and Cathode Materials[J].Chem. Rev. 2004, 104: 4271 – 4301.
[2]M.V. Reddy, G.V.Subba Rao, et al. metal Oxides and Oxysalts as Anode Materials for Li Ion Batteries[J]. Chem. Rev.2013, 113:5364?5457.
[3]Yoji Sakurai, Hajime Arai, Shigeto Okada, et al. Low temperature synthesis and electrochemical characteristics of LiFeO2 cathodes[J]. Journal of Power Sources.1997, 68:711-715.
[4]Ryoi Kanno, Takayuki Shirane, and Yoji Kawamoto. Synthesis, Structure, and Electrochemical Properties of a New Lithium Iron Oxide, LiFeO2, with a Corrugated Layer Structure[J].Electrochem. Soc.1996, 143: 2435-2442.
[5]Y.S. Lee, S. Sato, M. Tabuchi, C.S. Yoon d, et al.Structural change and capacity loss mechanism in orthorhombic Li/LiFeO2 system during cycling[J].Electrochemistry Communications.2003, 3: 549-554.
[6]Michele Catti, M.Merced Montero-Campillo.First-principles modelling of lithium iron oxides as battery cathode materials[J]. Journal of Power Sources.2011, 196: 3955-3961.
[7]A. Robert Armstrong, Daniel W. Tee, et al.Synthesis of Tetrahedral LiFeO2 and Its Behavior as a Cathode in Rechargeable Lithium Batteries [J]. J. American Chemical Society.2008, 130 : 3554-3559.
[8]Xiong Wang, Lisheng Gao, et al.Large-scale synthesis of a-LiFeO2 nanorods by low-temperature molten salt synthesis (MSS) method[J].Journal of Crystal Growth. 2004, 265 : 220–223.
[9]She-Huang Wu, Hsin-Yen Liu.Preparation of -LiFeO2-based cathode materials by an ionic exchange method[J].Journal of Power Sources, 2007, 174 : 789–794.
[10]Julian Morales, Jesus Santos-Pena.Highly electroactive nanosized a-LiFeO2[J]. Electrochemistry Communications. 2007, 9: 2116–2120.
[11]Masaaki Hirayama, Hiroki Tomita, Kei Kubota, et al.Structure and electrode reactions of layered rocksalt LiFeO2 nanoparticles for lithium battery cathode[J].Journal of Power Sources, 2011,196 :6809–6814.
[12]Haowen Liu, Panyin Ji, Xiaoyan Han.Rheological phase synthesis of nanosized a-LiFeO2 with higher crystallinity degree for cathode material of lithium-ion batteries[J].Materials Chemistry and Physics. 2016,183 :152-157.
[13]Zhi-jia Zhang, Jia-Zhao Wang, et al.Polypyrrole-coated -LiFeO2 nanocomposite with enhanced electrochemical properties for lithium-ion batteries[J].Electrochimica Acta. 2013,108: 820–826.
[14]Y.S. Lee, S. Sato, Y.K. Sun, K. Kobayakawa, Y. Sato.Preparation of Mn-substituted LiFeO2: A solid solution of LiFeO2 and LixMnO2[J].Electrochemistry Communications. 2003, 5: 359–364.
[15]Takashi MATSUHARA, Yuka TSUCHIYA, Keisuke YAMANAKA, Kei MITSUHARA, Toshiaki OHTA, Naoaki YABUUCHI.Synthesis and Electrode Performance of Li4MoO5-LiFeO2 Binary System as Positive Electrode Materials for Rechargeable Lithium Batteries[J].The Electrochemical Society of Japan,2016, 84: 797–801.
[16]P. Suresh, A.K. Shukla, N. Munichandraiah.Synthesis and characterization of LiFeO2 and LiFe0.9Co0.1O2 as cathode materials for Li-ion cells[J].Journal of Power Sources, 2006,159:1395–1400.
[17]A. K. Padhi, K.S. Nanjundaswamy, J.B.Goodenough. Phospho-olivines as Positive-Electrode Materials for Rechargeable Lithium Batteries[J]. J. Electrochem Soc, 1997, 144:1188-1194.
[18]Li-Xia Yuan, Zhao-Hui Wang, Wu-Xing Zhang, et al.Development and challenges of LiFePO4 cathode material for lithium-ion batteries[J].Energy Environ. Sci., 2011, 4: 269–284.
[19] Masaya Takahashi, Shinichi Tobishima, et al. Characterization of LiFePO4 as the cathode material for rechargeable lithium batteries[J]. Journal of Power Sources, 2001,98:508-511.
[20] Satish Bolloju , Rupesh Rohan, Shao-Tzu Wu. A green and facile approach for hydrothermal synthesis of LiFePO4 using iron metal directly[J]. Electrochimica Acta, 2016, 220:164–168.
[21] Xiaohui Tian, Yingke Zhou, Guan Wu. Controllable synthesis of porous LiFePO4 for tunable electrochemical Li-insertion performance[J]. Electrochimica Acta, 2017, 229: 316–324.
[22] Chao Gao, Jian Zhou, Guizhen Liu, and Lin Wang. Microwave-assisted synthesis and surface decoration of LiFePO4 hexagonal nanoplates for lithium-ion batteries with excellent electrochemical performance[J]. J. Mater Sci. 2017, 52:1590–1602.
[23]Xiaofeng Tu, Yingke Zhou, Yijie Song. Freeze-drying synthesis of three-dimensional porous LiFePO4 modified with well-dispersed nitrogen-doped carbon nanotubes for high-performance lithium-ion batteries[J]. Applied Surface Science. 2017, 400:329–338.
[24] Pier Paolo Prosini, Daniela Zane, Mauro Pasquali. Improved electrochemical performance of a LiFePO4 –based composite cathode[J]. Electrochimica Acta, 2001, 46:3517–3523.
[25] Adriyan Milev, Laurel George, Sourav Khan, et al. Li-ion kinetics in LiFePO4 /carbon nanocomposite prepared by a two-step process: The role of phase composition[J]. Electrochimica Acta. 2016, 209 :565–573.
[26] Jian-Wei Zhao, Shi-Xi Zhao, Xia Wu, Hong-Mei Cheng, Ce-Wen Nan. Double role of silicon in improving the rate performance of LiFePO4 cathode materials[J]. Journal of Alloys and Compounds. 2017, 699: 849-855.
[27] Huseyin Goktepe, Halil S, et al. Effect of silver and carbon double coating on the electrochemical performance of LiFePO4 cathode material for lithium ion batteries[J]. Hydrogen Energy, 2016, 41:9774-9779.
[28] Ian D. Johnson Ekaterina Blagovidova, Paul A. Dingwall. High power Nb-doped LiFePO4 Li-ion battery cathodes; pilot-scale synthesis and electrochemical properties[J]. Journal of Power Sources. 2016, 326: 476-481.
[29] Rakesh Saroha, Amrish K. Panwar, Yogesh Sharma. Development of surface functionalized ZnO-doped LiFePO4 /C composites as alternative cathode material for lithium ion batteries[J]. Applied Surface Science, 2017, 394:25–36.
[30] Theivanayagam Muraliganth, Arumugam Vadivel Murugan. Facile synthesis of carbon-decorated single-crystalline Fe3O4 nanowires and their application as high performance anode in lithium ion batteries[J]. Chem. Commun., 2009, 10:7360–7362.
[31] Guangmin Zhou, Da-Wei Wang, Feng Li, et al. Graphene-Wrapped Fe3O4 Anode Material with Improved Reversible Capacity and Cyclic Stability for Lithium Ion Batteries[J]. Chem. Mater. 2010, 22:5306–5313.
[32] Keyan Li, Hao Chen, Fenfen Shua, et al. Facile synthesis of iron-based compounds as high performance anode materials for Li-ion batteries. RSC Advances. 2014, 4: 36507–36512.
[33] Yaxiong Yang, Yongfeng Liu,et al. Highly Stable Cycling of Amorphous Li2CO3–Coated α-Fe2O3 Nanocrystallines Prepared via a New Mechanochemical Strategy for Li-Ion Batteries[J]. Adv. Funct. Mater. 2017, 27:1-10.


